昨日(2023年7月19日),據外媒醫療器械網報道,美國FDA已將頂級械企美敦力旗下植入式除顫器設備召回列為最嚴重的 I 級,意味著系列設備可能引發嚴重傷害或死亡。

FDA報告顯示,本次召回涉獵甚廣,涵蓋2017 年之后制造的所有帶有玻璃饋通的 ICD 和 CRT-D,數量高達348616臺。
這也是美敦力該系列設備上市以來最大規模的召回。
據了解,ICD 和 CRT-D 是植入心臟的設備,有助于監測和調節心律,當心臟進入不規則節律時,設備會檢測到不同步的心跳并產生電擊。
本次設備召回主要為設備能量輸出不穩定所致,也就是說,當需要高壓治療時,由于短路保護(SCP)功能的不當激活,系列設備可能會提供低能量或無能量輸出。
這樣一來將很有可能致使心臟驟停,目前系列設備已造成22人受傷。
本次召回具體產品信息如下:

設備名稱:
Cobalt XT、Cobalt、Crome ICD 和 CRT-D
Claria MRI、Amplia MRI、Compia MRI、Viva、Brava CRT-Ds
Visia AF、Visia AF MRI、Evera、Evera MRI、Primo MRI、Mirro MRI ICD
分發日期:2017年10月13日至2023年6月9日

美敦力 (Medtronic) 的 Colbalt XT ICD 和 CRT-D
針對該問題,美敦力以向客戶發出醫療器械緊急整改通知,并表示將對所有治療區域中的所有高壓治療路徑B>AX進行重新編程。
值得一提的是,本月早些時候,美敦力心臟設備數據平臺還因被發現嚴重網絡安全漏洞而遭到FDA的警告,(相關閱讀:美敦力被警告,涉嫌嚴重安全漏洞!)但該安全隱患現已通過軟件更新得以解決。
據流行病學調查顯示,心臟性猝死(sudden cardiac death, SCD)占各類猝死的80%以上。
由于SCD發病突然、不易及時發現并搶救,導致存活率極低,SCD已成為嚴重威脅人類公共衛生健康的定時炸彈。
除顫器的出現則讓人類在同“死神”對峙時不再處于絕對劣勢,從而有了回旋的余地。
“生死時速”間,既是生存所需、也是市場藍海,屆時頭部械企們紛紛加入這一戰壕,美敦力便是其中之一。
經過長達10年的研發投入,1996年,美敦力第一臺植入式心臟復律除顫器問世,然而還未來得及享受勝利的果實,大批故障問題便接踵而來。
這也波及到了中國市場的兩萬多臺設備。
2023年5月30日,國家藥監局發布消息,美敦力主動召回在華銷售的23803臺除顫器設備,召回原因正是此次FDA通報的能量輸送問題。

實際上,像近日這般動輒涉及幾萬、幾十萬臺設備的大規模召回并非獨一次,在兩年前(2021年)的239171臺設備一級召回中,系列產品涉訴高達444起,18人受傷。
據FDA報告顯示,該次召回為電池問題引發。
據了解,由于短路問題,會導致電池壽命縮短,繼而會觸發電池電量低的首次警告。如果用戶不響應該警告,設備可能會停止運行。
有關研究表示,除顫設備使用后大約三年后,這一問題的出現幾乎是“恒定的”,也就是說未來除顫器的大規模召回仍會時有發生。
伴隨著人口老齡化問題日益尖銳,除顫器市場規模與日俱增。
據貝哲斯市場調研報告數據顯示,2022年全球除顫器市場規模已達到1002.88億元(人民幣),中國除顫器市場規模達到254.43億元。
預計到2028年,全球除顫器市場規模將發展到1563.68億元。
然而值得一提的是,盡管在全球醫械市場上美敦力雄踞一方、名號最為響亮,然而在千億除顫領域上,這位械企“一哥”并非首屈一指。
早在1956年,保羅 · 卓爾(Paul Zoll)研制了世界上第一臺心臟除顫器,也正是這位哈佛醫學院教授在1980年創立了卓爾醫療。
據了解,卓爾醫療是全球首家全線除顫產品通過美國FDA的PMA批準的公司,現今仍是急危重癥護理及相關軟件和診斷工具領域的全球領導者。
在我國市場上,卓爾醫學也表現不俗,據華經產業研究院、浙商證券研究所統計,2019年我國除顫儀市場競爭格局中,卓爾醫學占比16%。
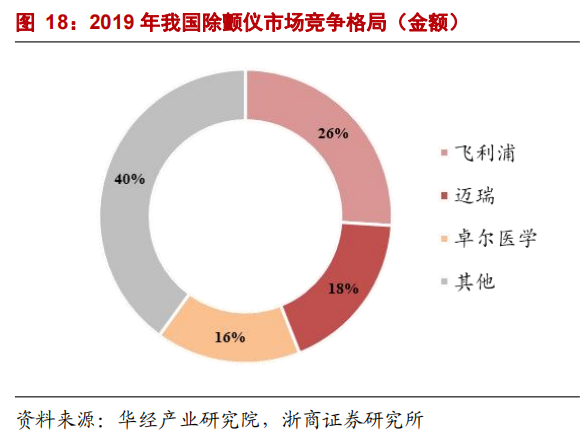
此外,綜合性械企巨頭們近年也頻頻在在急救設備市場涉足,除美敦力外,飛利浦、波士頓科學、百多力、雅培等近年來也不斷有新品推出,系列設備已陸續在全球市場上市。
2016年,在這之中雅培更是以250億美元(約合人民幣1791億元)的價格收購圣猶達醫療,強勢擴張了除顫器業務。
而國內市場中,也不斷有國產面孔在此展露頭角,其中最出色的當屬邁瑞醫療,生命信息與支持正是其三大業務之一,近年來在邁瑞在國內市場份額占比已經超過了卓爾醫學。
在全球醫械“內卷化”的當下,除顫器市場的械企們正在迎來新一輪較量,可以確定的是,作為和生死直接掛鉤的醫療設備,功能佳、故障少、安全性強的設備將會更得用戶青睞。
那么美敦力能否在本次大批召回后徹底解決除顫器的故障“頑疾”?除顫市場又將呈現哪些新局面?我們拭目以待。
(文章來源于互聯網)




 全部商品分類
全部商品分類