符合下列情形的醫療器械審查,適用于創新醫療器械特別審查程序:
(一)申請人通過其主導的技術創新活動,在中國依法擁有產品核心技術發明專li權,或者依法通過受讓取得在中國發明專li權或其使用權,創新醫療器械特別審查申請時間距專li授權公告日不超過5年;或者核心技術發明專li的申請已由國務院專li行政部門公開,并由國家知識產權局專li檢索咨詢中心出具檢索報告,報告載明產品核心技術方案具備新穎性和創造性。
(二)申請人已完成產品的前期研究并具有基本定型產品,研究過程真實和受控,研究數據完整和可溯源。
(三)產品主要工作原理或者作用機理為國內首創,產品性能或者安全性與同類產品比較有根本性改進,技術上處于國際領先水平,且具有顯著的臨床應用價值。
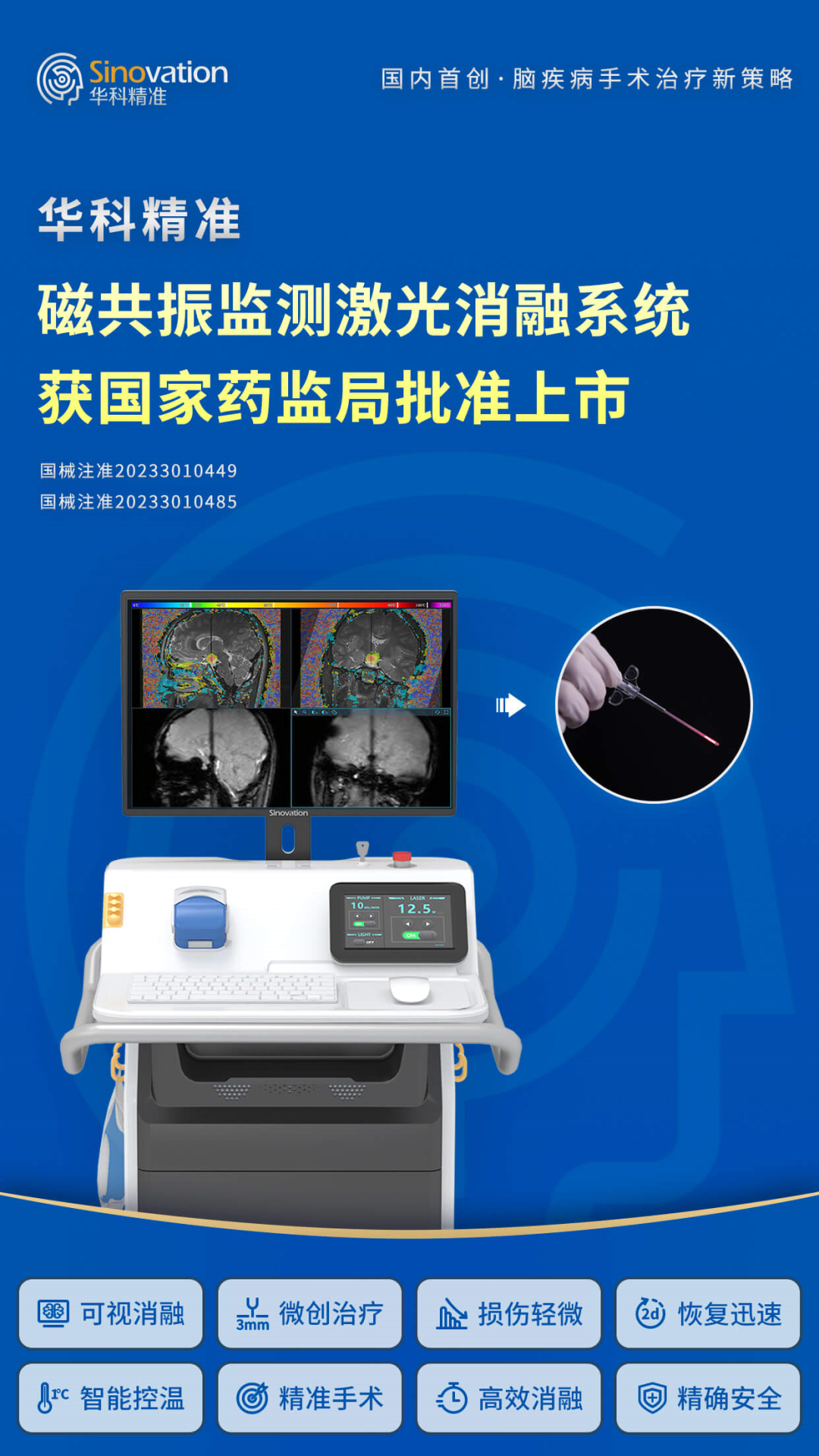
創新醫療器械產品解析 01 磁共振監測半導體激光治療設備 一次性使用激光光纖套件

產品概覽
產品名稱:磁共振監測半導體激光治療設備
生產企業:華科精準(北京)醫療科技有限公司
批準日期:2023/4/4
國械注準:20233010449
產品由主機和配件組成。配件包括傳輸光纖、耦合器、遙控聯鎖、防護眼鏡和腳踏開關。本產品與一次性使用激光光纖套件(LS-T1)配合,用于對藥物難治性癲癇患者(局灶性發作,有明確的致癇區部位或明確的癲癇傳導途徑)的局部病灶進行激光治療,包括 2 歲以上的下丘腦錯構瘤所致癲癇患者、5 歲以上的局灶性皮質發育不良所致癲癇患者以及 18 歲以上的顳葉內側癲癇患者。
該產品與一次性使用激光光纖套件配合使用。產品與磁共 振設備和一次性使用激光光纖套件連接,光纖置入病灶區域后, 將激光能量傳遞到周邊組織。在治療過程中,產品實時接收梯 度回波序列用于計算治療區域溫度并顯示,形成對治療過程的 實時監控。醫生參考圖像信息,調整激光功率和治療時間,實現對顱內病灶組織的精準治療。
產品名稱:一次性使用激光光纖套件
生產企業:華科精準(北京)醫療科技有限公司
批準日期:2023/4/13
國械注準:20233010485
產品由散射光纖、冷卻裝置(冷卻套管、冷卻循環管)和導向骨釘裝置組成。本產品與磁共振監測半導體激光治療設備(LS1)配合使用, 用于對藥物難治性癲癇患者(局灶性發作,有明確的致癇區部 位和明確的癲癇傳導途徑)的局部病灶進行激光治療,包括 2 歲以上的下丘腦錯構瘤所致癲癇患者、5 歲以上的局灶性皮質發 育不良所致癲癇患者以及 18 歲以上的顳葉內側癲癇患者。該產 品屬于磁共振環境條件安全醫療器械。
該產品與磁共振監測半導體激光治療設備配合使用。產品 組成中的冷卻循環管和冷卻套管形成保護散射光纖的水冷卻循 環,導向骨釘用于引導套管沿預定路徑置入。散射光纖末端通 過微加工工藝形形成橢球形出光區域,增加治療范圍、降低激光功率密度提高安全性。
02 冠狀動脈CT血流儲備分數計算軟件

產品概覽
產品名稱:冠狀動脈CT血流儲備分數計算軟件
生產企業:上海博動醫療科技股份有限公司
批準日期:2023/4/4
國械注準:20233210450
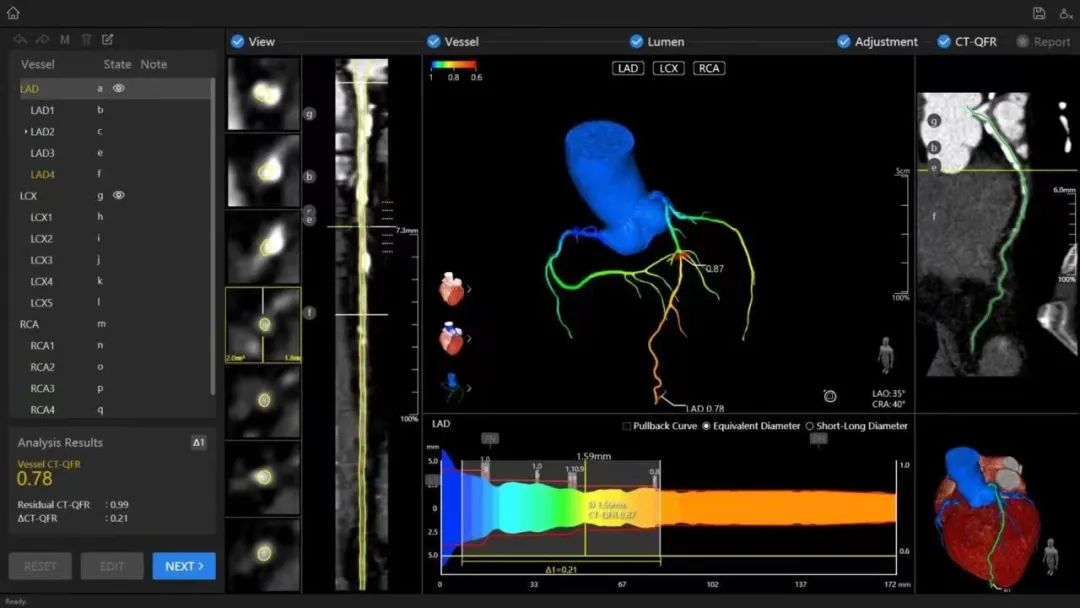
該產品由安裝程序、授權文件組成。功能模塊包括用戶登 錄、圖像查看、DICOM圖像導入、血管提取、血管輪廓提取、 管腔調整、CT-QFR分析和報告模塊。該產品基于冠脈CT血管造影圖像計算獲得CT血流儲備分 數,在進行冠脈血管造影檢查之前,輔助培訓合格的醫技人員 評估穩定性冠心病(SCAD)患者的功能性心肌缺血癥狀。臨床醫 生還應結合患者的病史、癥狀以及相關診斷結果進行綜合評判。該產品不適用于急性冠脈綜合征(ACS)等急性胸痛患者。
產品對CT設備造影增強圖像數據(CTA)進行冠狀血管樹 的三維重建,基于CTA數據計算血流分數(CT-QFR),獲取冠 脈血管上每個位置對應的CT-QFR數值,幫助臨床醫生判斷冠脈 狹窄是否引起心肌缺血,確定患者是否需要進一步進行介入檢查和治療。
03 冠狀動脈功能測量系統

產品概覽
產品名稱:冠狀動脈功能測量系統
生產企業:蘇州潤邁德醫療科技有限公司
批準日期:2023/4/20
國械注準:20233210219
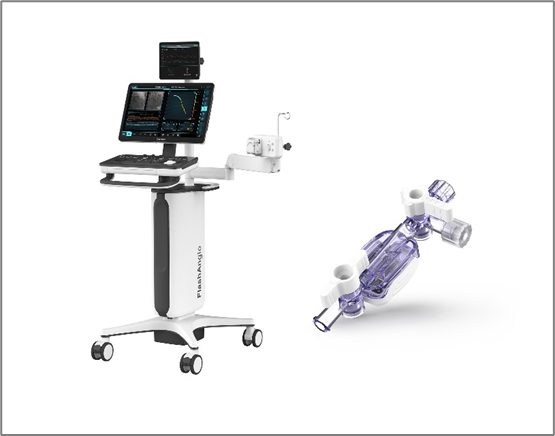
該產品由工作站、傳感器支架、IBP導聯線、IBP信號輸入 電纜(選配)組成。該產品僅限與蘇州潤邁德醫療科技有限公司的一次性使用 有創壓力傳感器配合使用,基于冠狀動脈血管造影影像計算冠 狀動脈造影血流儲備分數(coronary angiography Fractional Flow Reserve,caFFR)以及冠狀動脈造影微循環阻力指數(coronary angiography Index of Microcirculatory Resistance,caIMR),預 期供培訓合格的醫生用于成人患者冠狀動脈病變血管的功能學評價。
caIMR用于穩定性心絞痛、不穩定性心絞痛、疑診心肌缺血,冠狀動脈狹窄程度小于50%的無心肌病或阻塞性心外膜冠 狀動脈疾病的原發性冠狀動脈微血管功能障礙患者提供是否存在微循環阻力指數(IMR)大于等于或小于25的二分類評估, caIMR不能獨立用于心肌缺血的診斷,臨床中還應結合患者的臨 床病史、癥狀、其他診斷結果和臨床醫生的專業判斷進行綜合評價。
本產品通過對冠狀動脈造影影像進行血管分割、三維重建、 獲取血流速度,結合有創壓力傳感器測量的主動脈壓進行血流 動力學分析,實現對冠脈血管的冠狀動脈造影微循環阻力指數 (caIMR)的評估。
04 自膨式可載粒子膽道支架

產品概覽
產品名稱:自膨式可載粒子膽道支架
生產企業:南京融晟醫療科技有限公司
批準日期:2023/5/11
國械注準:20233130621
該產品由內、外支架組成,各帶有一個一次性使用置入器。外支架帶有粒子囊。一次性使用置入器由軟頭、內管、中管、外 管、前手柄、后手柄、助推管等組成。產品環氧乙烷滅菌,一次 性使用,貨架有效期 2 年。該產品用于因惡性腫瘤導致的無法手術或者不愿手術切除 的膽道狹窄/梗阻的擴張及治療。
該產品在內窺鏡和/或 X 射線的引導下,將支架放置至梗阻 部位進行擴張引流,同時利用放射性粒籽源 125I(不包含在產品 中)進行管腔內近距離放療,以抑制和破壞腫瘤細胞的生長。
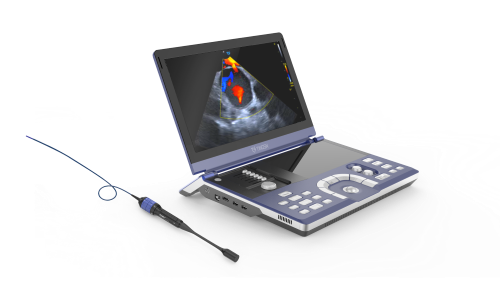
05 血管內成像設備 一次性使用血管內成像導管

產品概覽
產品名稱:血管內成像設備
生產企業:Conavi Medical Inc.
批準日期:2023-5-16
國械注進:20233060200
該產品由控制臺(ADM)和患者接口模塊(PIM)組成。該產品與同公司生產的一次性使用血管內成像導管(TA-06- 0001)配合使用,用于在醫療機構中需要進行冠狀動脈介入治療 患者的冠狀動脈成像,包括血管內超聲成像(IVUS)和血管內光 相干斷層成像(OCT)。配用的一次性使用血管內成像導管的 OCT 成像功能適用的冠脈血管直徑范圍是 2.0-4.0mm,不適用 于左冠狀動脈主干或以前做過旁路手術的目標血管。
血管內成像設備與血管內成像導管連接配合使用,用于在 進行經皮冠狀動脈介入手術時對冠狀動脈進行血管內成像。成 像設備通過探頭接口單元控制成像導管的探頭 360°旋轉和回撤, 通過成像段完成對血管的掃描。同時,成像設備發射近紅外光和超聲波,干涉儀和超聲模塊記錄不同深度血管的反射光和超 聲反射,設備重建反射光信號和超聲反射信號,形成血管內光 學干涉斷層圖像和血管內超聲圖像。
產品名稱:一次性使用血管內成像導管
生產企業:Conavi Medical Inc.
批準日期:2023-8-1
國械注進:20233060333
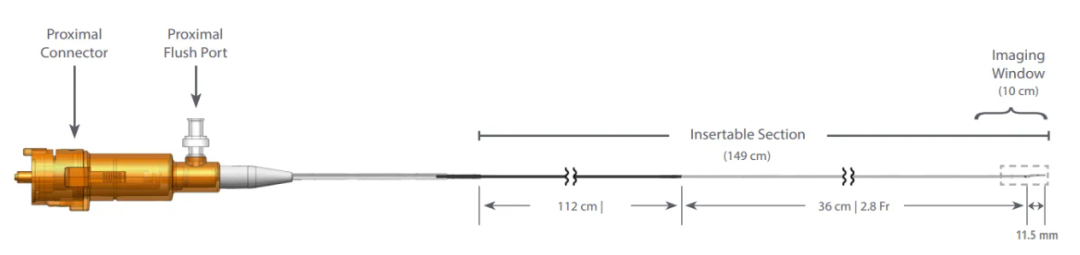
該產品由近端連接器(含沖洗孔)、外管和探頭組成。該產品與本公司生產的血管內成像設備(其中控制臺型號:TA-03-0005)配合使用,用于在醫療機構中需要進行冠狀動脈介 入治療患者的冠狀動脈成像,包括血管內超聲成像(IVUS)和血 管內光相干斷層成像(OCT)。一次性使用血管內成像導管的 OCT 成像功能適用的冠脈血管直徑范圍是 2.0-4.0mm,不適用 于左冠狀動脈主干或以前做過旁路手術的目標血管。
血管內成像導管與血管內成像設備連接配合使用,用于在 進行經皮冠狀動脈介入手術時對冠狀動脈進行血管內成像。成 像設備控制臺通過患者接口模塊控制成像導管的探頭 360°旋轉 和回撤,通過成像段完成對血管的掃描。同時,成像設備發射近 紅外光和超聲波,通過成像導管傳遞至血管,經反射后返回。干涉儀和超聲模塊記錄不同深度血管通過導管后的反射光和超聲 反射,成像設備重建反射光信號和超聲反射信號,形成血管內 光學干涉斷層圖像和血管內超聲圖像。
06 冠狀動脈介入手術控制系統 一次性使用冠狀動脈介入手術控制系統附件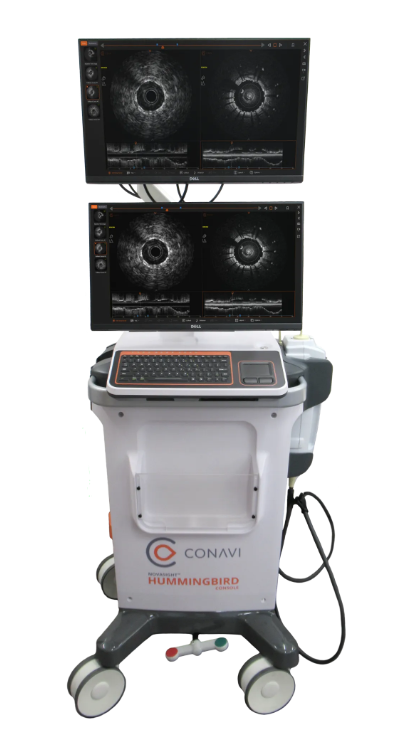


產品概覽
產品名稱:冠狀動脈介入手術控制系統
生產企業:Corindus Inc
批準日期:2023-6-1
國械注進:20233010225
產品由控制臺(301)、機械驅動臂(303)、延伸臂(312)、 介入屏蔽艙(101,選配)和顯示器(103/104,選配)組成。該產品在醫療機構使用,與本公司生產的一次性使用冠狀 動脈介入手術控制系統附件(盒帶、驅動齒輪)配合,輔助臨 床醫師用于經皮冠狀動脈介入手術期間,輸送和操作導絲、導 引導管、快速交換球囊擴張導管/支架。產品使用前應經過具有 資質的臨床醫師按目前診療指南對患者嚴重程度及病變復雜程 度進行判斷,對于高危患者或復雜病變需由臨床醫師嚴格按照 術前評估來判斷是否適用。不可用于急診。
本產品為冠脈介入手術中使用的控制系統,操作者在介入 屏蔽艙內或其他射線屏蔽環境下通過操作控制臺上的按鍵和滾 輪,來驅動機械臂及其末端安裝的配套附件,使得操作者無需在床旁即可實現對導絲、導管等介入器械的操控,從而避免或 減少操作者受到的輻射傷害。系統可實現導絲、導管的線性和旋轉運動,以及球囊和支 架的線性運動。具有 6 項 TechnIQ 功能,通過固定式的操作組合來實現模擬操作者的特定操作方式,以滿足部分場景所需的 自動化操作需求。系統在輸送介入器械的同時,可記錄并測量 運動距離,以評價血管相應部位的尺寸。系統還可基于驅動裝 置和傳動裝置的運動差異,監測器械是否出現受阻或打滑,并給出相應提示。
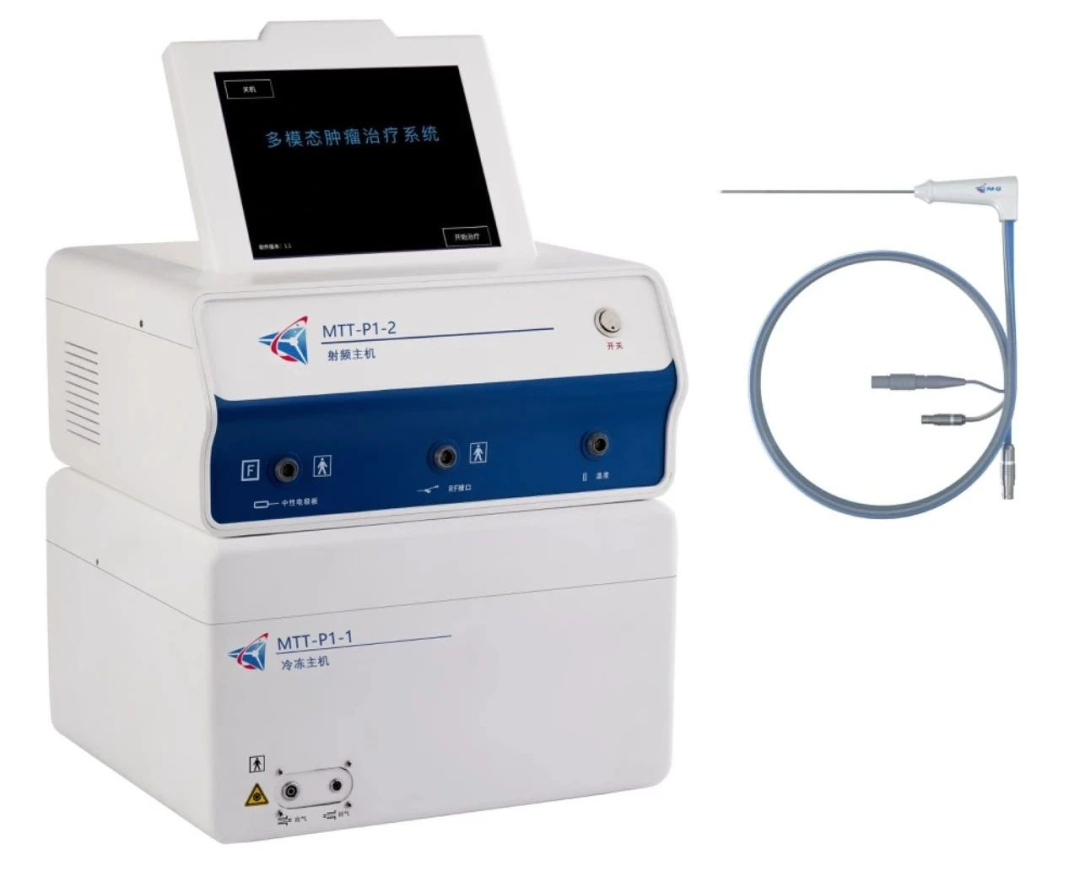
產品名稱:一次性使用冠狀動脈介入手術控制系統附件 生產企業:Corindus Inc 批準日期:2023-6-1 國械注進:20233010225 產品由盒帶和驅動齒輪組成。該產品在醫療機構使用,與本公司生產的冠狀動脈介入手 術控制系統(CorPath GRX System)配合,輔助臨床醫師用于 經皮冠狀動脈介入手術期間,輸送和操作導絲、導引導管、快 速交換球囊擴張導管/支架。產品使用前應經過具有資質的臨床 醫師按目前診療指南對患者嚴重程度及病變復雜程度進行判 斷,對于高危患者或復雜病變需由臨床醫師嚴格按照術前評估 來判斷是否適用。不可用于急診。 本產品為冠狀動脈介入手術控制系統配套的一次性使用無 源附件,包括盒帶和驅動齒輪兩個部件,均由高分子材料制作 而成。盒帶外殼材料為聚碳酸酯,內部組件主要由乙縮醛、聚氨酯和聚碳酸酯制成;驅動齒輪由聚碳酸酯和乙縮醛制成。使 用時需安裝在控制系統的機械臂末端,并將導絲、導管等被控 制介入器械安裝在盒帶的特定區域位置,盒帶內的驅動部件在 控制系統的帶動下推動被控器械實現不同的運動。 07 植入式左心室輔助系統 產品概覽 產品名稱:植入式左心室輔助系統 生產企業:深圳核心醫療科技有限公司 批準日期:2023-6-5 國械注準:20233120716 該產品由植入部件、體外部件、手術附件組成,其中植入部件包括左心室輔助泵(Corheart 6)、頂環(即心尖縫合環,CH-ACC-01)、出口管(CH-OF-01),體外部件包括連接器保護套(CH-ACC-05)、控制器(CH-CON-01)、可充電鋰電池組(CH-BAT-01、CH-BAT-02)、電源適配器(CHPW-01)、充電座(CH-CHG-01)、通訊適配器(CH-COMM01,選配)、監視器(MIT-W101-A,選配)、隨身包(CHBG-01)、淋浴包(CH-BG-02),手術附件包括開孔刀(CHACC-03)、拉線刀(CH-ACC-02)、連接器密封套(CH-ACC04)。 與特定人工血管配套使用,為進展期難治性左心衰患者血液循環提供機械支持,用于心臟移植前或恢復心臟功能的過渡治療。供具備心臟移植條件與術后綜合護理能力的醫療機構使用,醫務人員、院外護理人員以及患者須通過相應培訓。抗凝治療不耐受患者禁用。 該產品以旁路方式與患者的左心室、主動脈相連,將血 液由心尖部位引入左心室輔助泵,由泵葉輪轉動產生的離心 力將血液從左心室輔助泵排出,經出口管注入主動脈,從而 支持患者血液循環。 08 多模態腫瘤治療系統 產品概覽 產品名稱:多模態腫瘤治療系統 生產企業:上海美杰醫療科技有限公司 批準日期:2023-6-8 國械注準:20233010773 該產品由射頻主機、冷凍主機、一次性使用多模態腫瘤治療 消融針、腳踏板、輔助連接線(溫度信號連接線、壓力信號連接 線、冷凍控制連接線、冷凍主機供電互聯線)組成。在醫療機構中使用,用于對肝臟惡性實體腫瘤進行消融治 療,腫瘤最大直徑≤3cm。 該產品是集液氮冷凍與射頻加熱于一體的多模態治療系統, 通過對目標病灶進行預冷凍,后續進行射頻加熱并對過程進行 精確控制,從而完成加熱區域與冷凍區域重合的多模態腫瘤消融。 09 植入式骶神經刺激器 植入式骶神經刺激延伸導線 植入式骶神經刺激電極 產品概覽 產品名稱:植入式骶神經刺激器 生產企業:杭州承諾醫療科技有限公司 批準日期:2023-6-14 國械注準:20233120807 產品由植入式骶神經刺激器、扭力螺絲刀組成。該產品與植入式骶神經刺激電極及植入式骶神經刺激延伸 導線配套使用,適用于骶神經電刺激,用于成人排尿控制的輔 助治療,用于保守治療無效或不耐受保守治療的患者的膀胱過 度活動癥的癥狀,包括急迫性尿失禁、明顯的尿急、尿頻。 產品名稱:植入式骶神經刺激延伸導線 生產企業:杭州承諾醫療科技有限公司 批準日期:2023-6-14 國械注準:20233120808 產品由植入式骶神經刺激延伸導線、硅膠護套、緊固螺釘組成。該產品與植入式骶神經刺激器及植入式骶神經刺激電極配 套使用,適用于骶神經電刺激,用于成人排尿控制的輔助治療, 用于保守治療無效或不耐受保守治療的患者的膀胱過度活動癥 的癥狀,包括急迫性尿失禁、明顯的尿急、尿頻。 產品名稱:植入式骶神經刺激電極 生產企業:杭州承諾醫療科技有限公司 批準日期:2023-6-14 國械注準:20233120809 該產品由植入式骶神經刺激電極(含指引鋼絲)、導引針、 扭力螺絲刀、穿刺工具、擴張工具、隧道針組成。該產品與植入式骶神經刺激器及植入式骶神經刺激延伸導 線配套使用,適用于骶神經電刺激,用于成人排尿控制的輔助 治療,用于保守治療無效或不耐受保守治療的患者的膀胱過度 活動癥的癥狀,包括急迫性尿失禁、明顯的尿急、尿頻。 植入式骶神經刺激器用以產生特定電脈沖信號,與植入式 骶神經刺激延伸導線及植入式骶神經刺激電極配套使用,將特 定電脈沖連續施加于特定骶神經,以此興奮或抑制神經通路, 調節異常的骶神經反射弧,進而影響并調節膀胱、尿道/肛門括 約肌、盆底等骶神經支配靶器官的功能。 10 靜脈支架系統 產品概覽 產品名稱:靜脈支架系統 生產企業:蘇州茵絡醫療器械有限公司 批準日期:2023-7-28 國械注準:20233131034 該產品由自膨式鎳鈦合金支架和輸送系統組成。自膨支架 由鎳鈦絲編織而成。輸送系統由內管組件、外鞘管、顯影環和 手柄組成。產品經環氧乙烷滅菌,一次性使用。貨架有效期為 三年。該產品預期在髂股靜脈內使用,用于治療非血栓性髂靜脈 壓迫綜合征和深靜脈血栓形成后綜合征。 編織支架被預先裝配進入輸送系統的外鞘管內;支架系統 從血管穿刺部位進入人體血管內;當進入病變區域,通過回撤 輸送系統的外鞘管同時推進內管,補償支架短縮,使支架準確 定位在病變部位,支架靠自擴張方式撐開狹窄的血管并永久留 置在人體血管內用以建立血流通路。 11 顱內取栓支架 產品概覽 產品名稱:顱內取栓支架 生產企業:急速醫療有限公司 批準日期:2023-8-17 國械注進:20233030369 該產品由頭端、絲網、推送軸、控制絲和手柄組成,編 織絲網的材料為帶鉭芯鎳鈦絲,其近端和遠端各安裝有一個 90%鉑/10%銥合金的顯影標記。產品環氧乙烷滅菌,一次性使用。該產品預期用于在癥狀發作 8 小時內移除缺血性腦卒中 患者頸內動脈、大腦中動脈 M1 和 M2 段、基底動脈中的血栓,從而恢復血流。不能使用靜脈組織型纖溶酶原激活物 (IVt-PA)或 IVt-PA 治療失敗的患者是該治療的人選。 該產品的目的是局部捕獲腦血栓然后將其取出,重建血流。該產品是在射線透視下,通過 微導管將其輸送至病變部位,然后釋放編織絲網至目標血管 中的血栓處。該產品的絲網在出微導管時能夠保持其未出微 導管時的收縮尺寸。當編織絲網的位置確定時,術者可通過 手柄使編織絲網膨脹開。編織絲網的直徑和徑向支撐力可通 過滑動手柄上的滑塊調節。嵌栓完成后,術者在回撤時可適度收縮編織絲網,預期降低徑向支撐力來減少對血管的損傷。編織絲網的閉合末端預期減少遠端栓塞的風險。編織絲網的每根絲都含鉭芯,預期增加可視性。 12 球囊型冷凍消融導管 冷凍消融設備 產品概覽 產品名稱:球囊型冷凍消融導管 生產企業:上海微創電生理醫療科技股份有限公司 批準日期:2023-8-23 國械注準:20233011225 該產品由球囊型冷凍消融導管、手動回縮器、同軸連接線纜和連接電纜組成。球囊型冷凍消融導管產品分為A型、B型,其中A型(普通型)根據球囊外徑不同,分為23mm、28mm兩種類型,且每種直徑區分有無表面測溫功能;B型(壓力監測型)球囊外徑為28mm,球囊內裝有壓力監測傳感器,且不具有表面測溫功能,根據Tip頭長度分為長Tip和短Tip兩種規格。該產品在醫療機構中使用,與該公司生產的冷凍消融設備配套使用,用于藥物難治性、復發性、癥狀性陣發性房顫的治療。 該產品與冷凍消融設備配合使用,制冷劑從冷凍消融設備中經過同軸連接線纜,到達消融導管的球囊區段,在球囊內氣化從而達到冷凍消融溫度。遠端球囊內埋置溫度傳感器用于監測消融過程中球囊內部的溫度,并通過附件連接電纜與冷凍消融設備實現電氣連接,將球囊溫度反饋至冷凍消融 設備,可使設備調節制冷劑流量輸出。A 型球囊(EPAM231 和 EPAM281)表面的多個測溫元件可以檢測到球囊貼靠組織對應部位的溫度信息,與之相連的導線將溫度信息轉換為電信息,并通過連接電纜傳遞至冷凍消融設備,用于監測貼靠組織部位的溫度。B 型球囊(EPBM280 和 EPBN280)內裝有壓力監測傳感器,實時監測球囊內部壓力,壓力信息傳輸至冷凍消融設備,進而實現球囊內部壓力的實時監測與調節功能。所有型號導管可通過旋轉手柄上調節旋鈕帶動手柄內拉線來控制頭端彎型雙向偏轉。 產品名稱:冷凍消融設備 生產企業:上海微創電生理醫療科技股份有限公司 批準日期:2023-8-23 國械注準:20233011226 該產品由冷凍消融設備主機、腳踏開關、夾式接地線、電源線和排氣軟管組成。本產品在醫療機構中使用,與本公司生產的球囊型冷凍消融導管配套使用,用于藥物難治性、復發性、癥狀性陣發性房顫的治療。具有多檔位消融目標溫度控制功能、實時監測球囊表面多路溫度、自動匹配多型號導管參數、提供球囊內壓力監測功能等特點。 該產品在冷凍消融過程中,液態制冷劑N2O從氣瓶中輸出,通過特制的超細氣管、同軸連接線纜、導管手柄到達球囊導管的冷凍段。消融時,在球囊導管的冷凍段內部,液態制冷劑蒸發,吸收冷凍段周圍組織的熱量,形成有效消融灶, 達到治療目的。蒸發的氣體通過導管手柄內部及同軸連接線纜內部的管腔返回至冷凍消融設備,冷凍消融設備將廢氣排入醫院的抽吸或排出系統。根據不同患者術中溫度下降情況,醫生可選擇消融所需的溫度。當監測到球囊內部的溫度低于設定值時,在設備進液壓力控制信號和排氣壓力控制信號協同作用下,控制進液閥門減少N2O制冷劑的釋放,使得球囊內溫度達到目標溫度值。反之當實際溫度高于目標溫度時,設備增大N2O制冷劑的釋放,將溫度穩定在預設范圍。 13 二尖瓣夾系統 產品概覽 產品名稱:二尖瓣夾系統 生產企業:上海捍宇醫療科技股份有限公司 批準日期:2023-9-07 國械注準:20233131292 二尖瓣夾系統由二尖瓣夾、輸送系統和跨瓣器組成。其中,輸送系統由輸送器、推送器、裝載器、導管鞘和擴張器組成。二尖瓣夾由鎳鈦合金、S31793 不銹鋼、聚醚醚酮、PET 這些患者的基礎疾病不應影響降低二尖瓣反流后帶來的臨床受益。此類心臟團隊成員需要包括有二尖瓣手術經驗的心臟外科醫生和有二尖瓣疾病治療經驗的心臟疾病專家。該 產 品 由 接 受 過 二 尖 瓣 修 復 手 術 和 準 確 使 用ValveClamp?系統相關知識培訓的醫生使用,還需要具備一名心臟超聲專科醫生。 二 尖 瓣 夾 系 統 采 用 經 導 管 二 尖 瓣 緣 對 緣 修 復 (Transcatheter Edge-to-Edge Repair, TEER)技術,通過微創 小切口經心尖介入治療方式將二尖瓣夾植入人體。二尖瓣夾 固定在輸送系統上,通過裝載器將二尖瓣夾裝載進入導管 鞘,輸送至二尖瓣瓣葉處,經超聲引導準確定位并夾持住二 尖瓣的前葉和后葉,使瓣葉緊密對接,然后操作輸送系統釋 放二尖瓣夾,從而達到降低二尖瓣反流的目的。 14 一次性使用心腔內超聲診斷導管 產品概覽 產品名稱:一次性使用心腔內超聲診斷導管 生產企業:江蘇霆升科技有限公司 批準日期:2023/11/28 國械注準:20233061761 產品由導管主體、操作手柄和連接器組成。該產品在醫療機構使用,配合本公司生產的便攜式彩色超聲診斷儀(型號:TINGSN FINDERS 1,軟件發布版本:1)使 用,適用于心臟及心臟大血管、心內解剖結構的超聲成像。 本產品為用于心臟內超聲成像的成像導管,經股靜脈穿刺建立通道后經血管送至心臟部位,與本公司生產的超聲診斷儀配合使用,換能器發射機械超聲波,聲波通過介質進行傳播,在密度發生變化的地方產生回波,然后將接收到的回波經計算機處理提供實時高分辨率的圖像信息。超聲成像部件采用相控陣換能器,陣元材料為壓電陶瓷,封裝于導管遠端頭端內部。除超聲換能器外,導管遠端頭端還安裝有溫度傳感器,用于感應導管頭端內部溫度。 15 經導管二尖瓣夾系統 產品概覽 產品名稱:經導管二尖瓣夾系統 生產企業:杭州德晉醫療科技有限公司 批準日期:2023/11/29 國械注準:20233131775 經導管二尖瓣夾系統由導引鞘、二尖瓣夾系統兩個部件組成。其中導引鞘包含 24F 調彎鞘和擴張器兩個組件。二尖瓣夾系統包含二尖瓣夾和輸送系統兩個組成部分,輸送系統包含裝載器組件、11F 調彎鞘、夾子輸送導管三個組成部分,其中裝載器組件包含套筒和裝載器兩個組成部分。產品經環氧乙烷滅菌,一次性使用,貨架有效期 3 年。 該產品采用經皮方式,適用于經心臟團隊評估后認為存在外科手術高風險,且二尖瓣瓣膜解剖結構適合的退行性二尖瓣反流(MR≥3+)患者。這些患者的基礎疾病不應影響降低二尖瓣反流后帶來的臨床受益。該類心臟團隊成員需要包括有二尖瓣手術經驗的心臟外科醫生和有二尖瓣疾病治療經驗的心臟疾病專家。該產品由接受過心臟介入導管技術(包括經房間隔穿刺術)培訓并經過準確使用本器械系統相關培訓的臨床醫生使用,還需要具備一名心臟超聲專科醫生。 經導管二尖瓣夾系統由導引鞘和二尖瓣夾系統組成,二尖瓣夾系統包含二尖瓣夾和輸送系統,二尖瓣夾固定在輸送系統上。在輸送二尖瓣夾系統之前,經股靜脈推進導引鞘,直至導引鞘頭端穿過房間隔并到達左心房,將擴張器撤出體外。然后將二尖瓣夾系統插入 24F 調彎鞘并推進以將二尖瓣夾輸送至左心房。在血管輸送過程中,二尖瓣夾在 24F 調彎鞘內,直至到達左心房才被推出。通過操控 24F 調彎鞘和輸送系統手柄的調彎和旋轉功能來調整二尖瓣夾的位置,二尖瓣夾經正確定位在二尖瓣瓣葉上,再通過操作夾子手柄的各功能鍵,對二尖瓣前葉和后葉進行抓捕,結合超聲影像及 X射線引導下確定抓捕成功后,將二尖瓣夾關閉然后釋放二尖瓣夾,最后將 24F 調彎鞘和輸送系統撤出體外。二尖瓣的前葉和后葉被二尖瓣夾夾持,形成“雙孔化”結構,實現“緣對緣”修復。 16 產品概覽 產品名稱:冷凍消融設備 生產企業:康灃生物科技(上海)股份有限公司 批準日期:2023/12/4 國械注準:20233011815 本產品由冷凍裝置、真空系統、低溫工質輸送回路和控制系統組成。其中,冷凍裝置由預冷回路、深冷回路、液氮存儲器組成,真空系統由真空泵、真空閥、真空傳感器、真空回路組成,低溫工質輸送回路由壓力傳感器、電磁閥組成,控制系統由工控機、監視器組成。本產品在醫療機構中使用,與本公司生產的球囊型冷凍消融導管配套使用,用于藥物難治性、復發性、癥狀性陣發性房顫的治療. 本產品與球囊型冷凍消融導管配合使用,將氮氣經熱交換器冷卻后輸送至球囊內腔,使與組織接觸的球囊產生低溫。復溫時,將常溫氮氣輸送至球囊,球囊升溫解凍,使球囊表面與組織脫離。 治療過程中,設備通過導管反饋的溫度,動態調控冷凍介質的壓力和流量,將球囊表面溫度維持在規定范圍內。同時,設備真空泵持續抽取導管外層管路內的空氣,使產品外層管路達到高真空的隔熱狀態,確保非消融區域的安全。 產品名稱:球囊型冷凍消融導管 生產企業:康灃生物科技(上海)股份有限公司 批準日期:2023/12/4 國械注準:20233011815 本產品由設備連接部件、操作控制部件和血液接觸部件組成。其中,設備連接部件由公接頭、柔性連接管、快插接頭、回氣連接管組成,操作控制部件由三通止血閥、魯爾接頭、調彎手柄組成,血液接觸部件由內球囊、外球囊、內管、回氣管、進氣管、調彎鞘、顯影環、末端組成。本產品在醫療機構中使用,與本公司生產的冷凍消融設備配套使用,用于藥物難治性、復發性、癥狀性陣發性房顫的治療。 本產品與冷凍消融設備配合使用,將氮氣經熱交換器冷卻后輸送至球囊內腔,使與組織接觸的球囊產生低溫。復溫時,將常溫氮氣輸送至球囊,球囊升溫解凍,使球囊表面與組織脫離。 治療過程中,設備通過導管反饋的溫度,動態調控冷凍介質的壓力和流量,將球囊表面溫度維持在規定范圍內。同時,設備真空泵持續抽取導管外層管路內的空氣,使產品外層管路達到高真空的隔熱狀態,確保非消融區域的安全。












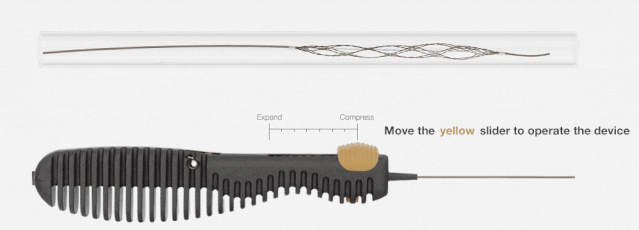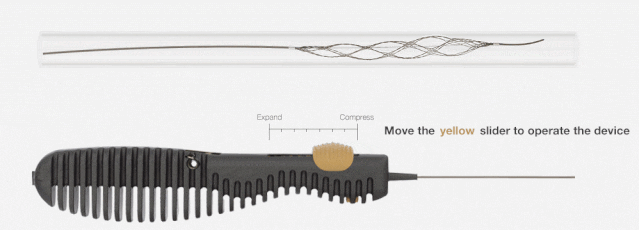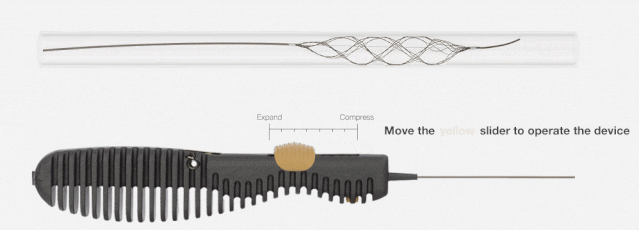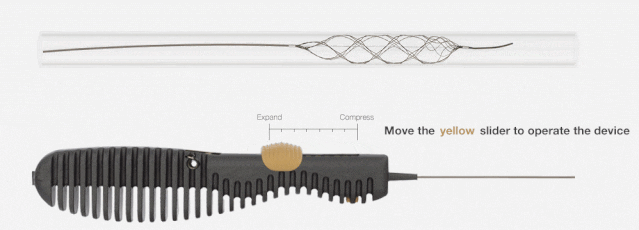






材料制成。產品經環氧乙烷滅菌,一次性使用,貨架有效期3 年。該產品采用經心尖手術方式,適用于經心臟團隊評估后認為存在外科手術高風險,且二尖瓣瓣膜解剖結構適合的退行性二尖瓣反流(MR≥3+)患者。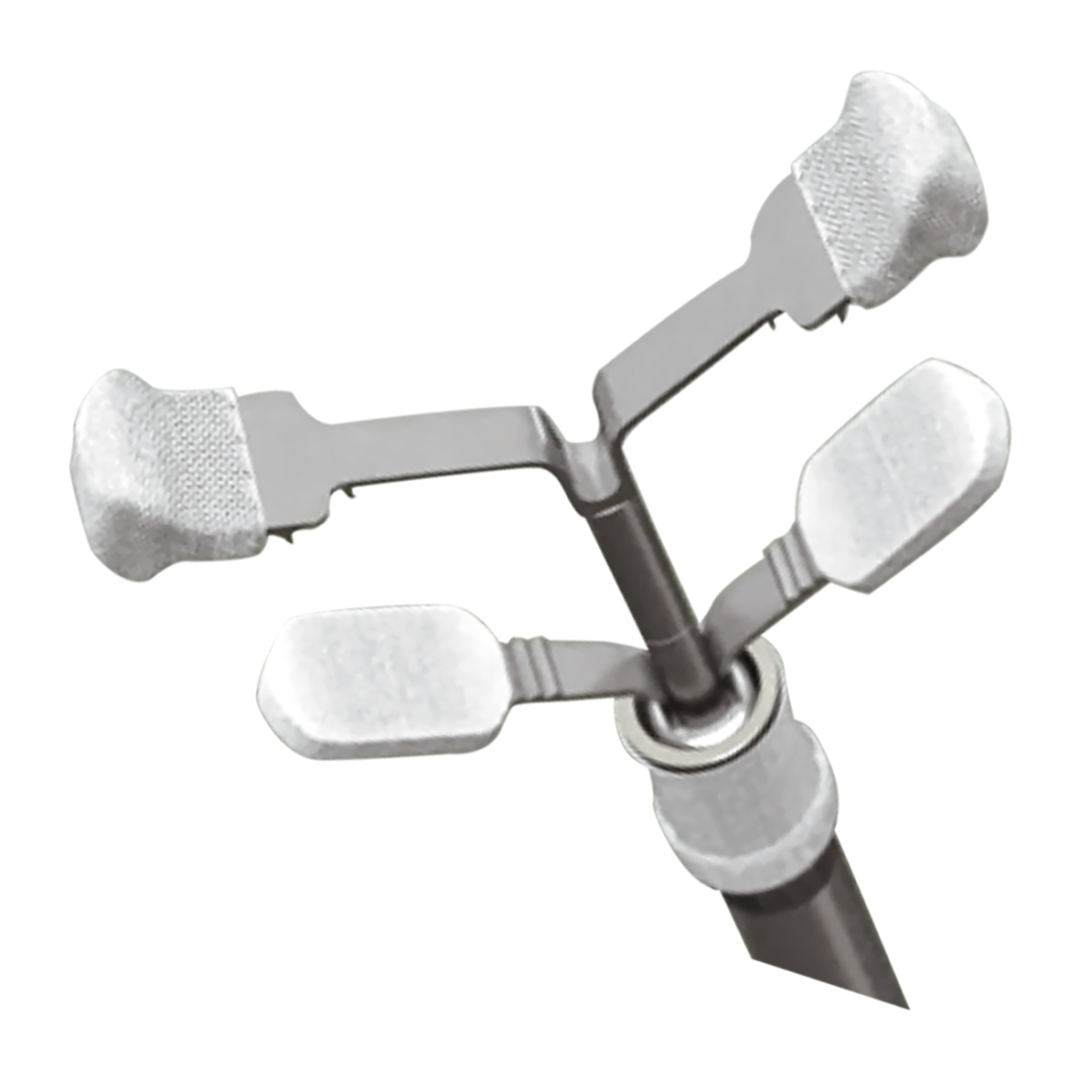








(文章來源于互聯網)




 全部商品分類
全部商品分類